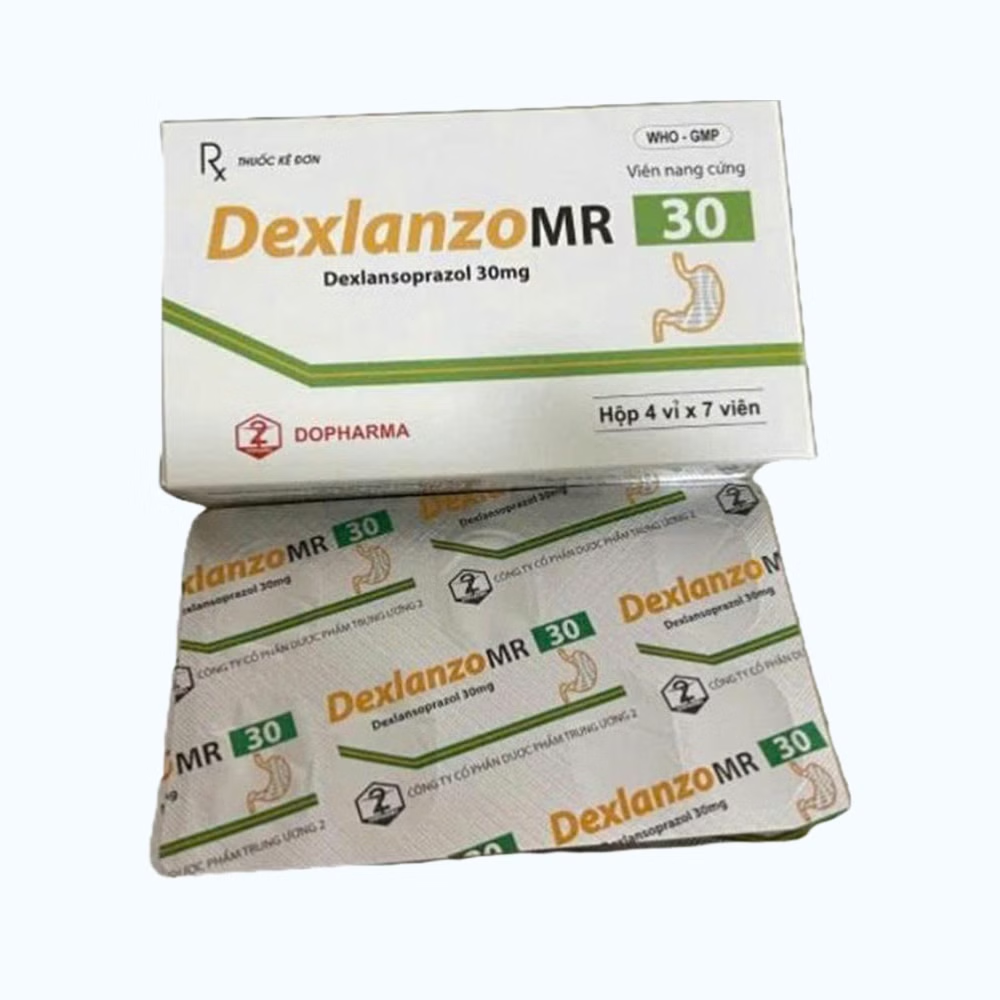
DexlanzoMR 30mg Dopharma (Hộp 28 Viên)
| Nhà sản xuất | Dopharma |
|---|---|
| Thuốc cần kê đơn | Có |
| Hoạt chất | Dexlansoprazol |
| Chỉ định | Viêm thực quản ăn mòn, chữa lành viêm thực quản ăn mòn và giảm ợ nóng, điều trị bệnh trào ngược dạ dày thực quản không ăn mòn có triệu chứng. |
| Đối tượng sử dụng | Người lớn và trẻ em từ 12 tuổi trở lên. |
| Dạng bào chế | Viên nang cứng chứa vi hạt bao tan trong ruột. |
| Quy cách | Hộp 04 vỉ x 07 viên |
| Mô tả ngắn | DexlanzoMR 30mg Dopharma điều trị viêm thực quản ăn mòn, chữa lành viêm thực quản ăn mòn và giảm ợ nóng, điều trị bệnh trào ngược dạ dày thực quản không ăn mòn có triệu chứng. |
| Lưu ý | Sản phẩm này chỉ bán khi có chỉ định của bác sĩ, mọi thông tin trên đây chỉ mang tính chất tham khảo. Vui lòng đọc kĩ thông tin chi tiết ở tờ hướng dẫn sử dẫn của sản phẩm. |
Thành phần
Dexlansoprazol 30mg
Công dụng
CHỈ ĐỊNH:
Chữa lành viêm thực quản ăn mòn: DexlanzoMR được chỉ định ở bệnh nhân từ 12 tuổi trở lên để chữa lành tất cả các cấp độ viêm thực quản ăn mòn (EE) trong tối đa 8 tuần.
Duy trì sự chữa lành viêm thực quản ăn mòn và giảm ợ nóng: DexlanzoMR được chỉ định ở bệnh nhân từ 12 tuổi trở lên để duy trì sự chữa lành viêm thực quản ăn mòn và giảm ợ nóng đến 6 tháng ở bệnh nhân người lớn và 16 tuần ở bệnh nhân từ 12- 17 tuổi.
Điều trị bệnh trào ngược dạ dày thực quản không ăn mòn có triệu chứng: DexlanzoMR được chỉ định ở bệnh nhân từ 12 tuổi trở lên để điều trị bệnh trào ngược dạ dày, thực quản (GERD) không ăn mòn có triệu chứng trong 4 tuần.
ĐẶC TÍNH DƯỢC LỰC HỌC:
Dexlansoprazol là một PPI ức chế sự tiết acid dạ dày bằng cách ức chế đặc hiệu (H +, K +) – ATPase trong tế bào thành dạ dày. Bằng cách tác động đặc biệt lên bơm proton, dexlansoprazol chặn bước cuối cùng của quá trình sản xuất acid.
ĐẶC TÍNH DƯỢC ĐỘNG HỌC:
Hấp thu:
Sau khi uống 30 mg hoặc 60 mg dexlansoprazol cho những người khỏe mạnh và bệnh nhân GERD có triệu chứng, giá trị trung bình của Cmax và AUC của dexlansoprazol tăng theo tỷ lệ tương ứng.
Phân bố:
Liên kết với protein huyết tương của dexlansoprazol dao động từ 96,1% đến 98,8% ở những người khỏe mạnh và không phụ thuộc vào nồng độ từ 0,01 đến 20 mcg mỗi ml. Thể tích phân bổ rõ ràng (Vz/F) sau nhiều liều ở bệnh nhân GERD có triệu chứng là 40,3 L
Chuyển hóa:
Dexlansoprazol được chuyển hóa rộng rãi ở gan bằng cách oxy hóa, khử và hình thành các liên hợp sulfat, glucuronid và glutathion sau đó thành các chất chuyển hóa không hoạt động. Các chất chuyển hóa oxy hóa được hình thành bởi hệ thống enzym cytochrom P450 (CYP) bao gồm hydroxyl hóa chủ yếu bởi CYP2C19, và oxy hóa thành sulfon bởi CYP3A4.
CYP2C19 là một enzym gan đa hình thể hiện ba kiểu hình trong quá trình chuyển hóa cơ chất CYP2C19; Chất chuyển hóa rộng rãi (* 1/* 1), chất chuyển hóa trung gian (* 1/ đột biến) và chất chuyển hóa kém (đột biến / đột biến). Dexlansoprazol là thành phần lưu thông chính trong huyết tương bất kể trạng thái chuyển hóa CYP2C19. Trong các chất chuyển hóa trung gian và rộng rãi CYP2C19, các chất chuyển hóa chính trong huyết tương là 5-hydroxy dexlansoprazol và liên hợp glucuronide của nó, trong khi ở các chất chuyển hóa kém CYP2C19 dexlansoprazol sulfon là chất chuyển hóa chính trong huyết tương.
Thải trừ:
Sau khi uống thuốc, không có dexlansoprazol chuyển hóa được bài tiết qua nước tiểu. Sau khi dùng [14C] dexlansoprazol cho 6 đối tượng nam khỏe mạnh, khoảng 50,7% (độ lệch chuẩn (SD): 9.0%) phóng xạ được sử dụng đã được bài tiết qua nước tiểu và 47,6% (SD: 7,3% trong phân. Độ thanh thải rõ ràng (CL/F) ở những người khỏe mạnh lần lượt là 11,4 đến 11,6 L/ giờ, sau 5 ngày sử dụng 30mg hoặc 60 mg mỗi ngày một lần.
Đối tượng đặc biệt Trẻ em
Dược động học của dexlansoprazol ở bệnh nhân dưới 12 tuổi chưa được nghiên cứu. Bệnh nhân từ 12 đến 17 tuổi
Dược động học của dexlansoprazol đã được nghiên cứu ở 36 bệnh nhân từ 12-17 tuổi bị bệnh trào ngược dạ dày-thực quản có triệu chứng trong một thử nghiệm đa trung tâm. Các bệnh nhân được chọn ngẫu nhiên để dùng dexlansoprazol 30 hoặc 60 mg, 1 lần/ngày trong 7 ngày. Cmax và AUC trung bình của dexlansoprazol ở các bệnh nhân từ 12-17 tuổi theo thứ tự là 105 và 88%, so với ở người lớn với liều 30mg và theo thứ tự là 81 và 78%, với liều 60 mg.
Bảng 2. Các thông số dược động học trung bình (% CV) ở bệnh nhân từ 12-17 tuổi có triệu chứng GERD vào ngày thứ 7 sau khi dùng dexlansoprazol một lần mỗi ngày trong 7 ngày
Liều dùng: 30 mg (N=17) – Cmax (ng/mL): 691 (53) – AUCtau (ng.h/mL): 2886 (47) – CL/F (L/h): 12.8 (48)
Liều dùng: 60 mg (N=18) – Cmax (ng/mL): 1136 (51) – AUCtau (ng.h/mL): 5120 (58) – CL/F (L/h): 15.3 (49)
Người cao tuổi
Thời gian bán thải pha cuối cùng của dexlansoprazol tăng đáng kể ở người cao tuổi so với các đối tượng trẻ hơn (tương ứng là 2,2 và 1,5 giờ). Dexlansoprazol cho thấy nồng độ toàn thân (AUC) cao hơn ở đối tượng lớn tuổi (cao hơn 34%) so với đối tượng trẻ hơn.
Giới tính
Trong một nghiên cứu trên 12 đối tượng nam và 12 nữ khỏe mạnh đã nhận một liều duy nhất dexlansoprazol 60 mg, nữ giới có mức tiếp xúc toàn thân (AUC) cao hơn (cao hơn 43%) so với nam giới. Sự khác biệt về mức độ phơi nhiễm giữa nam và nữ không thể hiện mối quan tâm đáng kể về an toàn.
Suy thận
Dexlansoprazol được chuyển hóa mạnh ở gan thành các chất chuyển hóa không có hoạt tính, và không tìm thấy thuốc ban đầu trong nước tiểu sau khi uống một liều dexlansoprazol. Do đó, dược động học của dexlansoprazol dự kiến sẽ không bị thay đổi ở bệnh nhân suy thận và không có nghiên cứu nào được tiến hành ở bệnh nhân suy thận. Ngoài ra, dược động học của lansoprazol không khác biệt trên mặt lâm sàng ở bệnh nhân suy thận nhẹ, trung bình hoặc nặng so với người khỏe mạnh có chức năng thận bình thường.
Suy gan
Trong một nghiên cứu trên 12 bệnh nhân bị suy gan trung bình (Child-Pugh nhóm B) uống một liều duy nhất 60 mg dexlansoprazol, nồng độ toàn thân (AUC) của dexlansoprazol liên kết và không liên kết với protein cao hơn khoảng hai lần so với người có chức năng gan bình thường. Sự khác biệt về mức độ phơi nhiễm này không phải do sự khác biệt về khả năng liên kết với protein. Không có nghiên cứu nào được thực hiện ở bệnh nhân suy gan nặng (Child-Pugh nhóm C).
Hướng dẫn sử dụng
LIỀU DÙNG:
Liều khuyến cáo ở bệnh nhân từ 12 tuổi trở lên
Bảng 1. Phác đồ liều khuyến cáo của viên nang DexlanzoMR theo chỉ định ở bệnh nhân từ 12 tuổi trở lên.
Chỉ định – Liều dùng – Thời gian điều trị:
*Chữa lành viêm thực quản ăn mòn (EE) – 60mg x 1 lần/ngày – Tối đa 8 tuần
*Duy trì sự chữa lành viêm thực quản ăn mòn và giảm ợ nóng – 30mgx1 lần/ngày – Các nghiên cứu có đối chứng không kéo dài qua 6 tháng ở bệnh nhân người lớn và 16 tuần ở bệnh nhân từ 12-17 tuổi.
Bệnh trào ngược dạ dày – thực quản (GERD) không ăn mòn có triệu chứng – 30mg x 1 lần/ngày – 4 tuần
Điều chỉnh liều ở bệnh nhân suy gan để chữa lành viêm thực quản ăn mòn (EE):
Đối với bệnh nhân suy gan trung bình (Child-Pugh nhóm B), liều khuyến cáo là 30 mg x 1 lần/ngày trong tối đa 8 tuần.
DexlanzoMR không được khuyến cáo sử dụng ở những bệnh nhân bị suy gan nặng (Child-Pugh
nhóm C).
Các đối tượng đặc biệt:
Trẻ em
Tính an toàn và hiệu quả của dexlansoprazol đã được thiết lập ở bệnh nhân nhi từ 12 tuổi đến 17 tuổi để chữa lành tất cả các loại EE, duy trì EE được chữa lành và giảm chứng ợ nóng, và điều trị chứng ợ nóng liên quan đến GERD không ăn mòn có triệu chứng.
Tính an toàn và hiệu quả của dexlansoprazol chưa được thiết lập ở bệnh nhi dưới 12 tuổi. Dexlansoprazol không được khuyến cáo ở bệnh nhi dưới hai tuổi (xem Cảnh báo và thận trọng). Các nghiên cứu tiền làm sàng ở chuột chưa trưởng thành được điều trị bằng lansoprazol (hỗn hợp racemic) đã chứng minh tác dụng phụ của việc làm dày van tim và thay đổi xương khi tiếp xúc với dexlansoprazol được cho là tương tự hoặc cao hơn mức tiếp xúc với dexlansoprazol ở bệnh nhi từ một đến hai tuổi.
Việc sử dụng dexlansoprazol không được khuyến cáo để điều trị GERD có triệu chứng ở bệnh nhi từ một tháng đến dưới một tuổi vì lansoprazol không được chứng minh là có hiệu quả trong một thử nghiệm mù đôi, đa trung tâm.
Người cao tuổi
Trong tổng số bệnh nhân (n=4548) trong các nghiên cứu lâm sàng về dexlansoprazol, 11% bệnh nhân từ 65 tuổi trở lên, trong khi 2% từ 75 tuổi trở lên, không có sự khác biệt tổng thể nào về tính an toàn hoặc hiệu quả được ghi nhận giữa những bệnh nhân này và bệnh nhân trẻ tuổi hơn. Các kinh nghiệm làm sáng được báo cáo khác đã không xác định được sự khác biệt đáng kể về đáp ứng giữa bệnh nhân cao tuổi và bệnh nhân trẻ tuổi, nhưng không thể loại trừ khả năng nhạy cảm cao hơn của một số người lớn tuổi.
Suy gan
Không cần điều chỉnh liều dexlansoprazol đối với bệnh nhân suy gan nhẹ (Child-Pugh Loại A). Trong một nghiên cứu trên những bệnh nhân trưởng thành bị suy gan mức độ trung binh (Child- Pugh Nhóm B) dùng một liều duy nhất 60 mg dexlansoprazol, đã có sự gia tăng đáng kể mức độ tiếp xúc toàn thân của dexlansoprazol so với những người khỏe mạnh có chức năng gan bình thường. Do đó, đối với những bệnh nhân bị suy gan trung bình (Child-Pugh Nhóm B), nên giảm liều để chữa bệnh EE (xem Liều dùng và cách dùng).
Không có nghiên cứu nào được thực hiện ở bệnh nhân suy gan nặng (Child-Pugh Loại C); việc sử dụng dexlansoprazol không được khuyến cáo cho những bệnh nhân này.
Suy thận
Dexlansoprazol được chuyển hóa mạnh ở gan thành các chất chuyển hóa không có hoạt tính, và không tìm thấy thuốc ban đầu trong nước tiểu sau khi uống một liều dexlansoprazol. Do đó, dược động học của dexlansoprazol dự kiến sẽ không bị thay đổi ở bệnh nhân suy thận và không có nghiên cứu nào được tiến hành ở bệnh nhân suy thận. Ngoài ra, dược động học của lansoprazol không khác biệt trên mặt lâm sàng ở bệnh nhân suy thận nhẹ, trung bình hoặc nặng so với người khỏe mạnh có chức năng thận bình thường.
Do vậy không cần điều chỉnh liều đối với bệnh nhân suy thận.
CÁCH DÙNG:
Thông tin quan trọng về cách dùng:
- Dùng không liên quan đến thức ăn.
- Quên liều: Nếu một lần quên không dùng thuốc, dùng lại càng sớm càng tốt. Tuy nhiên, nếu gần đến lịch của liều tiếp theo, không dùng liều đã quên mà dùng liều tiếp theo đúng giờ. Không dùng hai liều cùng một lúc để bù cho liều đã quên.
- Uống nguyên cả viên, không được nhai.
Đối với những bệnh nhân khó uống viên nang, có thể mở viên nang DexlanzoMR và uống cùng nước sốt táo như sau:
– Đặt một muỗng canh nước sốt táo vào một đồ chứa sạch.
– Mở viên nang.
– Rắc các hạt còn nguyên vẹn lên nước sốt táo.
– Uống nước sốt táo và các hạt ngay lập tức. Không nhai các hạt. Không lưu trữ nước sốt táo và hạt để sử dụng về sau.
Một cách khác, có thể uống viên nang cùng với nước qua một xy lanh uống (oral syringe) hoặc ống thông mũi-dạ dày (NG)
Dùng với nước qua một xy lanh uống
– Mở viên nang và đo các hạt vào một đồ chứa sạch có 20 ml nước.
– Rút toàn bộ hỗn hợp vào một xy lanh.
– Lắc nhẹ xy lanh để giữ các hạt khỏi lắng xuống.
– Đưa hỗn hợp vào miệng uống ngay lập tức. Không lưu trữ hỗn hợp nước và hạt để sử dụng về
sau.
– Làm đầy lại xy lanh với 10 ml nước, lắc nhẹ và uống.
– Làm đầy lại xy lanh một lần nữa với 10 ml nước, lắc nhẹ và uống.
Thận trọng
TÁC DỤNG KHÔNG MONG MUỐN CỦA THUỐC (ADR)
Tác dụng không mong muốn phổ biến nhất (2%)
- Ỉa chảy, đau bụng, buồn nôn, nhiễm trùng đường hô hấp trên, nôn mửa, đầy hơi.
- Tác dụng không mong muốn dẫn đến ngừng thuốc
- Trong các nghiên cứu lâm sàng có kiểm soát, phản ứng bất lợi phổ biến nhất dẫn đến ngừng điều trị dexlansoprazol là tiêu chảy (0,7%).
Tác dụng không mong muốn khác(<2%)
- Rối loạn hệ thống máu và bạch huyết: Thiếu máu, nổi hạch.
- Rối loạn tim: đau thắt ngực, rối loạn nhịp tim, nhịp tim chậm, đau ngực, phù, nhồi máu cơ tim, đánh trống ngực, nhịp tim nhanh.
- Rối loạn tai: đau tai, ù tai, chóng mặt.
- Rối loạn nội tiết: bướu cổ.
- Rồi loạn mắt: kích ứng mắt, sưng mắt.
- Rối loạn tiêu hóa: khó chịu ở bụng, đau bụng, phân bắt thường, khó chịu ở hậu môn, ruột có âm thanh bắt thường, mùi hơi thở, viêm đại tràng, viêm đại tràng co thắt, táo bón, khô miệng, khó tiêu polyp dạ dày, viêm dạ dày ruột, rỗi loạn tăng trương lực đường tiêu hóa, GERD, loét GI và thủng, chảy máu, tụ máu, trĩ, nôn mửa, dị cảm miệng, xuất huyết trực tràng.
- Rồi loạn chung và điều trị tại chỗ: phản ứng có hại của thuốc, suy nhược, đau ngực, ớn lạnh, cảm thấy bắt thường, viêm, viêm niêm mạc, nốt sản, đau.
- Rồi loạn gan mật: đau bụng đường mật, sỏi túi mật, gan to.
- Rối loạn hệ thống miễn dịch: quá mẫn.
- Nhiễm trùng: nhiễm nắm candida, cúm, viêm mũi họng, herpes miệng, viêm họng, viêm xoang, nhiễm virus, nhiễm trùng âm hộ-âm đạo.
- Rối loạn chuyển hóa và dinh dưỡng: thay đổi khẩu vị, tăng calci máu, hạkali máu.
CHỐNG CHỈ ĐỊNH:
Bệnh nhân mắn cảm với bắt kỳ thành phần nào của thuốc,
Bệnh nhân đang dùng sản phẩm chứa rilpiviin.
CẢNH BÁO VÀ THÂN TRỌNG KHI DÙNG THUỐC:
Sự hiện diện của khối u ác tính ở dạ dày.
Ở người lớn, đáp ứng về triệu chứng với điều trị bằng Dexlansoprazol không loại trừ sự hiện điện của bệnh ác tính ở dạ dày. Xem xét thêm xét nghiệm chẳn đoán và (heo dõi thêm ở những bệnh nhân trưởng thành có đáp ứng dưới mức tối ưu hoặc tái phát triệu chứng sớm sau khi hoàn thành điều trị bằng thuốc ức chế bơm proton (PP). Ở bệnh nhân cao tuổi, xem xét thêm việc nội soi.
Viêm thận kẽ cấp tính (TIN):
Việm thận kế cấp tịnh đã được quan sát ở bệnh nhân dùng PPI và có thể xảy ra tại bẮI kỷ thời điểm nào trong quá trình điểu trị bằng PP. Bệnh nhân có các dấu hiệu và triệu chứng khác nhau từ phản ứng quả mẫn có triệu chứng dẫn đến các triệu chứng không đặc hiệu của suy giảm chức năng thận (ví dụ: khó chịu, buồn nôn, chán ăn). Trong các trường hợp được bảo cáo, một số bệnh nhân được chẩn đoán bằng sinh thiết và không có biểu hiện ngoài thận (vi dụ: sốt, phát ban hoặc đau khớp). Ngừng dexlansoprazol và đánh giá bệnh nhân nghỉ ngờ mắc TIN cấp tính.
Tiêu chảy liên quan đền Clostridium difficile:
Các nghiên cửu quan sát đã công bổ gợi ý rằng liệu pháp PPI như dexlansoprazol có thẻ là tăng nguy cơ tiêu chảy do Clostridium difficile, đặc biệt ở bệnh nhân nằm viện. Chẩn đoán nên được xem xét đối với bệnh tiêu chảy không cải thiện (xem Tác dụng không mong muốn)
Bệnh nhân nên sử dụng liều thấp nhất và thời gian điều tị PPI ngắn nhát phủ hợp với tình trạng bệnh.
Gãy xương:
Một số nghiên cứu quan sát được công bồ cho tháy liệu pháp PPI có thẻ tăng nguy cơ gãy xương hông, cổ tay hoặc cột sống liên quan đắn loãng xương. Nguy cơ gãy xương tăng lên ở những bệnh nhân dùng liều cao, được định nghĩa là dùng nhiều liều hàng ngày và điều trị PPI dài hạn (một năm hoặc lâu hơn). Bệnh nhân nên sử dụng liều thắp nhất và thời gian điều trị PPI ngắn nhất phù hợp với tình trạng bệnh đang được điều trị. Bệnh nhân có nguy cơ bị gãy xương, loãng xương nên xử trí theo hướng dẫn điều trị đã được thiết lập (Xem Liều lượng và cách dùng, Tác dụng không mong muốn).
Các phần ứng có hại nghiêm trọng trên da
Các phản ứng bắt lợi nghiêm trọng trên da, bao gồm hội chứng Slevens-Johnson (SJS) và hoại tử biểu bì nhiễm độc (TEN), phản ứng thuốc với tăng bạch câu ái toan và các triệu chứng toàn thân (DRESS), hội chứng mụn mũ ngoại ban toàn thân cắp tính (AGEP) đã được báo cáo liên quan đến việc sử dụng PPI. Ngừng sử dụng dexlansoprazol khi có dấu hiệu hoặc triệu chứng đầu tiên của phản ửng bất lợi nghiêm trọng trên da hoặc các dầu hiệu quá mẫn khác và xem xót đánh giá thêm.
Lupus ban đỏ và toàn thân:
Lupus ban đỏ ở đa (CLE) và lupus ban đỏ hệ thống (SLE) đã được báo cáo ở những bệnh nhân dùng PPI. Những biến cố này vừa xảy ra dưới dạng khởi phát và đợt cấp của bệnh tự miễn hiện có. Đa số các trường hợp lupus ban đỏ do PPI là lupus ban đỏ ở da (CLE).
Dạng CLE thường gặp nhát được bảo cáo ở những bệnh nhân được điều tị bằng PPI là CLE bản cấp (SCLE) và xảy ra trong vòng vài tuần đến vài năm sau khi điều trị liên tục ở những bệnh nhân từ trẻ sơ sinh đến người cao tuổi. Nói chung, các phát hiện về mô học đã được quan sát thầy không có sự tham gia của cơ quan.
Lupus ban đỏ hệ thống (SLE) được báo cáo hơn so với lupus ban đỏ ở da ở những bệnh nhân dùng PPI. SLE liên quan đền PPI thường nhẹ hơn SLE không do thuốc. Khởi phát SLE thường xảy ra trong vòng vài ngày đến vài năm sau khi bắt đầu điều trị chủ yếu ở những bệnh nhân từ thanh niên đến người già. Phần lớn bệnh nhân có biểu hiện phát ban; tuy nhiên, đau khớp và giảm tế bảo máu cũng đã được báo cáo.
Tránh sử dụng PPI lâu hơn so với chỉ định y khoa. Nếu các dấu hiệu hoặc triệu chứng phù hợp với CLE hoặc SLE được ghi nhận ở những bệnh nhân dùng dexlansoprazol, hãy ngừng thuốc và chuyển bệnh nhân đến bác sĩ chuyên khoa thích hợp đề đánh giá. Hầu hét bệnh nhân cải thiện khi ngừng PPI đơn thuần trong vòng 4 đến 12 tuần. Xét nghiệm huyết thanh học (ví dụ: ANA) có thể dương tính và kết quả xét nghiệm huyết thanh học tăng cao có thể mất nhiều thời gian hơn để cải thiện so với các biểu hiện lâm sàng.
Thiếu Cyanocobalamin (Viamin B12):
Điều trị hàng ngày với bất kỳ loại thuốc ức chế axit nào trong một thời gian dài (ví dụ: hơn ba năm) có thể dẫn đền tình trạng kém hấp thu cyanocobalamin (Vitamin B12) do quá ít hoặc giảm tiết axit dạ dày. Hiếm có báo cáo vẻ sự thiếu cyanocobalamin xảy ra với liệu pháp ức chế axit đã được báo cáo trong y văn. Chẩn đoán này nên được xem xét nếu các triệu chứng lâm sàng phù hợp với sự thiếu cyanocobalamin được quan sát thấy ở những bệnh nhân được điều trị bằng
dexiansoprazol.
Hạ magie máu và chuyển hóa khoáng chất:
Hạ magie máu, có tiệu chứng và không có triệu chứng, hiếm khi được báo cáo ở những bệnh nhân được điều trị bằng PPI trong ít nhất ba tháng, trong hầu hết các trường hợp sau một năm điều trị. Các tác dụng ngoại ý nghiêm trọng bao gồm co cứng cơ, rối loạn nhịp tìm và co giật. Hạ magie máu có thể dẫn đến hạ canxi máu và/hoặc hạ kali máu.
Đối với những bệnh nhân dự kiến sẽ điều trị kéo dài hoặc những người dùng thuốc ức chế bơm proton cùng với thuốc như digoxin hoặc thuốc có thể gây hạ magie máu (ví dụ: thuốc lợi tiểu) các nhân viên y tế có thể cân nhắc theo dõi nồng độ magie trước khi bắt đầu điều trị bằng thuốc ức chế bơm proton và theo dõi định kỳ (xem Tác dụng không mong muốn).
Cân nhắc theo dõi nồng độ magie và canxi trước khi bắt đâu dùng dexlansoprazol và định kỳ trong quá trình điều tị ở những bệnh nhân có nguy cơ hạ canxi máu từ trước (ví dụ, suy tuyến cận giáp). Bổ sung magie và/hoặc canxi khi cần thiết. Nếu hạ canxi máu khó điều trị, hãy xem xét ngừng thuốc ức chế bơm proton..
Tương tác với xét nghiệm chuẩn đoán khối u thần kinh:
Nồng độ CgA tăng thứ phát do giảm axit dạ dày do PPI. Nồng độ CgA tăng có thể gây ra kết quả dương tính giả trong điều tra chẩn đoán cho khối u thần kinh.
Tạm thời ngừng điều trị Dexlansoprazol ít nhất 14 ngày trước khi đánh giá mức độ CgA và xem xét lặp lại xét nghiệm nếu nồng độ CgA ban đầu cao. Nếu các thử nghiệm nối tiếp được thực hiện(ví dụ: để theo dõi), cùng một phòng thí nghiệm thương mại nên được sử dụng để thử nghiệm vì phạm vi tham chiếu giữa các thử nghiệm có thể khác nhau
Tương tác với methotrexat:
Y văn cho thầy rằng việc sử dụng đồng thời PPI với methotrexat (chủ yếu ở liều cao) có thể làm tăng và kéo dài nồng độ methotrexat và/hoặc chất chuyển hóa của nó trong huyết thanh, có thể dẫn đến ngộ độc methotrexat. Khi sử dụng methotrexat liều cao, có thể cân nhắc tạm thời ngừng PPI ờ một số bệnh nhân (xem Tương tác thuốc).
Polyp tuyến đáy vị:
Việc sử dụng PPI có liên quan đền việc tăng nguy cơ polyp tuyến đảy vị khi sử dụng lâu dài, đặc biệt là sau một năm. Hầu hết những người sử dụng PPI phát triển polyp tuyến đáy vị đều không có triệu chứng và polyp tuyến đáy vị được xác định tình cờ khi nội soi. Sử dụng liệu pháp PPI trong thời gian ngắn nhất phù hợp với tình: tạng đang được điều trị.
Nguy cơ dày van tim ở bệnh nhỉ dưới hai tuổi:
Viên nang giải phóng chậm dexlansoprazol không được khuyến cáo ở bệnh nhi dưới hai tuổi. Các nghiên cứu tiền lâm sàng ở chuột chưa trưởng thành với lansoprazol đã chứng minh tác dụng phụ làm dày van tim. Dexlansoprazol là đồng phân đói hình của lansoprazol.
Dùng với nước qua một ống thông mũi-dạ dày (cỡ >16 French).
– Mở viên nang và đổ các hạt vào một đồ chứa sạch có 20ml nước.
– Rút toàn bộ hỗn hơp vào một xy lanh có đầu ống thông.
– Lắc nhẹ xy lanh để giữ các hạt khỏi lắng xuống và bơm ngay hỗn hợp qua ống thông mũi-dạ dày vào trong dạ dày. Không lưu trữ hỗn hợp nước vả hạt để sử dụng vẻ sau.
Làm đầy lại xy lanh có đầu ống thông một lần nữa với 10 ml nước, lắc nhẹ và súc rửa ống thông.
Làm đầy lại xy lanh có đầu ống thông một lần nữa với 10 ml nước, lắc nhẹ và sử dụng.
SỬ DỤNG THUỐC CHO PHỤ NỮ CÓ THAI VÀ CHO CON BÚ:
Thời kỳ mang thai:
Không có nghiên cứu với việc sử dụng dexlansoprazol ở phụ nữ mang thai để thông báo nguy cơ liên quan đến thuốc, nên chỉ sử dụng dexlansoprazol khi mang thai nếu cân thiết rõ ràng.
Thời kỳ cho con bú:
Không có thông tin liên quan đền sự hiện diện của dexlansoprazol trong sữa mẹ, ảnh hưởng đến trẻ sơ sinh bú sữa mẹ hoặc ảnh hưởng đền sản xuất sữa. Tuy nhiên, lansoprazol và các chất chuyển hóa của nó có trong sữa chuột. Lợi ích phát triển và sức khỏe của việc cho con bú nên được xem xét cùng với nhu câu lâm sàng của người mẹ đổi với dexlansoprazol và bất kỳ tác dụng phụ tiềm ẳn nào đối với đứa trẻ được nuôi bằng sữa mẹ từ dexlansoprazol hoặc tử tình trạng bà mẹ tiểm ẩn.
ẢNH HƯỚNG CỦA THUỐC LÊN KHẢ NĂNG LÁI XE, VẬN HÀNH MÁY MÓC:
Chưa có bằng chứng về ảnh hưởng của thuốc lên khả năng lái xe và vận hành máy móc.
TƯƠNG TÁC, TƯƠNG KỴ CỦA THUỐC:
Thuốc kháng retrovirus:
Tác dụng của PPI đối với thuốc kháng vi-rút là khác nhau. Tầm quan trọng lâm sàng và các cơ chế đằng sau những tương tác này không phải lúc nào cũng được biết đến.
Giảm tiếp xúc với một số loại thuốc kháng virus (ví dụ, rilpivirin, atazanavir và nelfinavir) khi sử dụng đồng thời với dexlansoprazol có thể làm giảm tác dụng kháng virus và thúc đẩy sự phát triển của kháng thuốc.
Tăng phơi nhiễm của các thuốc kháng retrovirus khác (ví dụ, saquinavir) khi sử dụng đồng thời với dexlansoprazol có thể làm tăng độc tinh của thuốc kháng retrovirus.
Có những loại thuốc kháng retrovirus khác không dẫn đến tương tác lâm sàng với dexlansoprazol. Các sản phẩm có chứa rilpivirin: Sử dụng đồng thời với dexlansoprazol bị chống chỉ định.
Warfarin:
Tăng chỉ số INR và thời gian prothrombin ở bệnh nhân dùng PPI và warfarin đồng thời. Tăng chỉ số INR và thời gian prothrombin có thể dẫn đến chảy máu bất thường và thậm chí tử vong. Theo dõi chỉ số INR và thời gian prothrombin. Điều chỉnh liều của warfarin có thể cần thiết để duy trì phạm vi mục tiêu INR. Xem thông tin kê đơn cho warfarin.
Methotrexat:
Sử dụng đồng thời PPI với methotrexat (chủ yếu ở liều cao) có thể làm tăng và kéo dài nồng độ methotrexat trong huyết thanh và / hoặc chất chuyển hóa hydroxymethotrexat của nó, có thể dẫn đến độc tính của methotrexat. Không có nghiên cứu tương tác thuốc chính thức của methotrexat liều cao với PPI đã được tiến hành. Việc rút tạm thời dexlansoprazol có thể được xem xét ở một số bệnh nhân dùng methotrexat liều cao.
Digoxin:
Làm tăng cường khả năng tiếp xúc của thuốc. Theo dõi nồng độ digoxin. Điều chỉnh liều digoxin có thể cẫn thiết để duy trì nồng độ thuốc điều trị. Xem thông tin kê đơn cho digoxin.
Thuốc phụ thuộc vào pH dạ dày để hấp thu (ví dụ: muối sắt, erlotinib, dasatinib, nilotinib, mycophenolat mofetil, ketoconazol/itraconazol):
Dexlansoprazol có thể làm giảm sự hấp thu của các loại thuốc khác do tác dụng của nó trong
việc giảm độ acid trong dạ dày.
Mycophenolat mofetil (MMF). Phối hợp PPI ở những người khỏe mạnh và ở những bệnh nhân cấy ghép nhận MMF đã được báo cáo để giảm tiếp xúc với chất chuyển hóa hoạt động, acid mycophenolic (MPA), có thể do giảm khả năng hòa tan MMF ở dạ dày pH. Sự liên quan lâm sàng a giảm phơi nhiễm MPA khi thải ghép nội tặng chưa được thiết lập ở những bệnh nhân ghép tạng được điều trị bằng dexlansoprazol và MMF. Sử dụng dexlansoprazol một cách thận trọng ở những bệnh nhân cấy ghép nhận MMF
Xem thông tin kê đơn cho các thuốc khác phụ thuộc vào pH dạ dày để hấp thu.
Tacrolimus:
Có khả năng tăng tiếp xúc của tacrolimus, đặc biệt ở những bệnh nhân cấy ghép, chất chuyển hóa trung gian là CYP2C19.
Theo dõi nồng độ tacrolimus trong máu. Điều chỉnh liều của tacrolimus có thể cần thiết để duy tri nồng độ thuốc điều trị. Xem thông tin kê đơn cho tacrolimus.
Tương tác với xét nghiệm chuẩn đoán khối u thần kinh:
Nồng độ CgA tăng thứ phát do giảm axit dạ dày do PPI. Nồng độ CgA tăng có thể gây ra kết quả dương tính giả trong điều tra chẩn đoán cho khối u thần kinh.
Tạm thời ngừng điều trị dexlansoprazol ít nhất 14 ngày trước khi đánh giá mức độ CgA và xem xét lặp lại xét nghiệm nếu nồng độ CgAban đầu cao. Nếu các thử nghiệm nối tiếp được thực hiện (ví dụ: để theo dõi), cùng một phòng thí nghiệm thương mại nên được sử dụng để thử nghiệm, vì phạm vi tham chiếu giữa các thử nghiệm có thể khác nhau.
Tương tác với thử nghiệm kích thích secretin
Tăng phản ứng trong bài tiết gastrin để đáp ứng với xét nghiệm kích thích secretin, gợi ý sai lệch về bệnh viêm dạ dày.
Tạm thời ngừng điều trị dexlansoprazol it nhất 30 ngày trước khi đánh giá để cho phép mức gastrin trở về mức cơ bản.
Xét nghiệm nước tiểu dương tính giả cho THC
Đã có bảo cáo về xét nghiệm sàng lọc nước tiểu dương tính giả đối với tetrahydrocannabinol (THC) ở bệnh nhân dùng PPI.
Một phương pháp xác nhận thay thế nên được xem xét để xác minh kết quả tích cực.
Thông tin sản xuất
Bảo quản: Bảo quản nơi khô, nhiệt độ dưới 30 độ C, tránh ánh sáng
Nơi sản xuất: Việt Nam
Nhà sản xuất: Dopharma
Quy cách: Hộp 04 vỉ x 07 viên.
| Nhà sản xuất | Dopharma |
|---|---|
| Thuốc cần kê đơn | Có |
| Hoạt chất | Dexlansoprazol |
| Chỉ định | Viêm thực quản ăn mòn, chữa lành viêm thực quản ăn mòn và giảm ợ nóng, điều trị bệnh trào ngược dạ dày thực quản không ăn mòn có triệu chứng. |
| Đối tượng sử dụng | Người lớn và trẻ em từ 12 tuổi trở lên. |
| Dạng bào chế | Viên nang cứng chứa vi hạt bao tan trong ruột. |
| Quy cách | Hộp 04 vỉ x 07 viên |
| Mô tả ngắn | DexlanzoMR 30mg Dopharma điều trị viêm thực quản ăn mòn, chữa lành viêm thực quản ăn mòn và giảm ợ nóng, điều trị bệnh trào ngược dạ dày thực quản không ăn mòn có triệu chứng. |
| Lưu ý | Sản phẩm này chỉ bán khi có chỉ định của bác sĩ, mọi thông tin trên đây chỉ mang tính chất tham khảo. Vui lòng đọc kĩ thông tin chi tiết ở tờ hướng dẫn sử dẫn của sản phẩm. |










Đánh giá
Chưa có đánh giá nào.